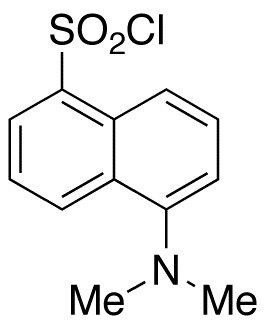
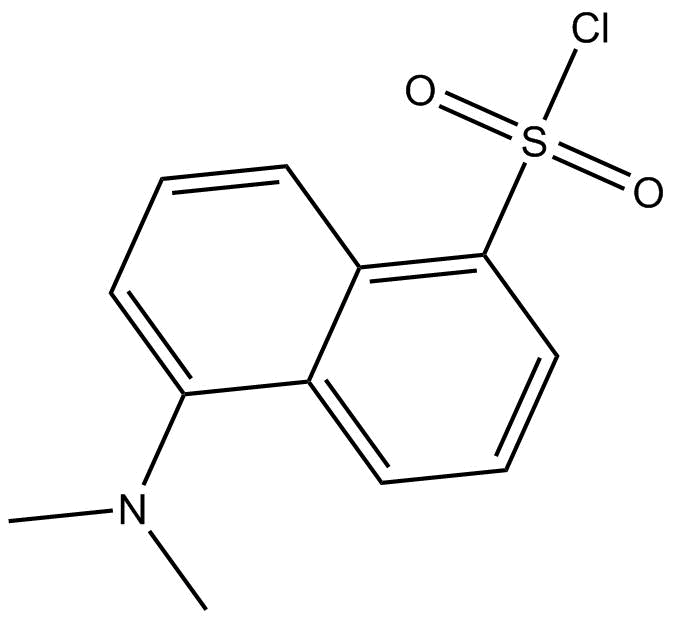
Dansylchlorid, chemisch: 5-(Dimethylamino)naphthalin-1-sulfonylchlorid, wird als Reagenz auf primäre aliphatische und aromatische Aminogruppen eingesetzt. Es bildet mit diesen stabile blau- oder blaugrün fluoreszierende Sulfonamide. Dansylchlorid ist ein vielverwendetes Hilfsmittel in der Endgruppenbestimmung von Peptiden und in der Aminosäureanalyse. Es wurde erstmals von Gregorio Weber Anfang der 1950er-Jahre synthetisiert.
Anwendungsprinzip in der Endgruppenbestimmung von Peptiden
Dansylchlorid reagiert mit endständigen Aminogruppen in Peptiden und bildet Addukte von hoher Hydrolysestabilität. Die nachfolgende Hydrolyse der Peptidaddukte führt daher zur Spaltung der Peptidbindungen, wobei das Addukt aus endständiger Aminosäure und Dansylchlorid erhalten bleibt und chromatographisch charakterisiert werden kann.
Anwendung in der Flexibilitätsuntersuchung von Proteinen
Die mit Aminosäuren gebildeten Sulfonamide sind im Allgemeinen gute Akzeptoren für Förster-Resonanzenergietransfer (FRET) in Kombination mit der Aminosäure Tryptophan, was die Markierung mit Dansylchlorid zu einem geeigneten Mittel zur Untersuchung der Flexibilität von Proteinen macht. Die Zugabe von β-Cyclodextrin (Cycloheptaamylose) verstärkt die Resonanz der Sulfonamid-Addukte.
Chemische Eigenschaften
Dansylchlorid ist instabil in Dimethylsulfoxid (DMSO), das daher nicht als Lösungsmittel für das Reagenz geeignet ist.
Einzelnachweise

.jpg)
